- Доктор Матар
- Детская андрология
- Детская хирургия
- Детская урология
- Услуги
- Операции
- Галерея
- Андрология в картинках
- Анатомия мужской половой системы
- Анатомия яичка
- Аорто-мезентериальная вилка (схема)
- Баланопостит
- Варикоцеле
- Водянка оболочек яичка (Гидроцеле) у детей
- Паховая грыжа у детей
- Киста семенного канатика
- Крипторхизм
- Мочевые пути человека (верхние)
- Мочевые пути человека (нижние)
- Источники кровоснабжения яичка
- Обрезание
- Общая схема мужской мочеполовой системы
- Скрытый половой член
- Фимоз
- Укус полового члена
- Гипоспадия
- Гипоспадия типа хорды
- Меатостеноз
- Родителям
- Центр
- Вопрос - ответ
- Статьи
- Отзывы
- Контакты
Диагностика и лечение нейрогенных дисфункций мочевого пузыря у детей
 ДИАГНОСТИКА И ЛЕЧЕНИЕ НЕЙРОГЕННЫХ ДИСФУНКЦИЙ МОЧЕВОГО ПУЗЫРЯ У ДЕТЕЙ
ДИАГНОСТИКА И ЛЕЧЕНИЕ НЕЙРОГЕННЫХ ДИСФУНКЦИЙ МОЧЕВОГО ПУЗЫРЯ У ДЕТЕЙ
В основе дисфункций мочеиспускания одной из наиболее частых причин обращения детей в нефрологической практике лежат, как правило, функциональные нарушения механизмов накопления и опорожнения мочевого пузыря без предлежащих неврологических и травматических повреждений. Данные состояния способны вызывать повреждения верхних отделов мочевой системы вплоть до развития необратимых почек, поэтому требуют комплексного подхода как в отношении клинико-инструментального обследования, так и лечебной тактики.
Impaired mechanisms of accumulation and emptying of the bladder without predisposing neurological and traumatic injuries are generally responsible for dysuria, a most common cause of children's referral in nephrological care.
These conditions may cause upper urinary diseases, even by causing irreversible renal changes since they require a comprehensive approach to be used both in clinical and instrumental studies and treatment.
В.И. Кириллов, профессор. Кафедра детских болезней Московского медицинского стоматологического института
Н.Г. Киреева, врач-ординатор. Московская городская детская больница Святого Владимира
Prof. V.I.Kirilov, Department of Childhood Diseases, Moscow Medical Stomatological Institute
N.G.Kireyeva, Registrar, Saint Vladimir City Children's Hospital, Moscow
Ввиду неясности этиологии функциональных расстройств мочевого пузыря и нередкого отсутствия их инструментального подтверждения для их обозначения используют самые разнообразные термины: синдромы дисфункционального мочеиспускания, ненейрогенный нейрогенный мочевой пузырь, субклинический нейрогенный мочевой пузырь, оккультный нейропатический мочевой пузырь и др. В основе многих дисфункций мочеиспускания, по крайней мере тех, которые могут привести к повреждениям верхних отделов мочевого тракта, лежит недостаточность координации активности детрузора, шейки мочевого пузыря или наружного сфинктера. Указанные нарушения встречаются либо изолированно, либо в комбинации и часто приводят к повышению внутрипузырного давления без явных неврологических предлежащих патологических процессов.
Патогенез
Мочеиспускание является сложным актом, и зрелый его режим включает координированную функцию ряда мышечных образований, когда волевое сокращение детрузора сопровождается расслаблением наружного сфинктера с опорожнением мочевого пузыря под относительно низким давлением [1]. У новорожденных и детей первых месяцев жизни мочеиспускание является непроизвольным, с замыканием дуг рефлексов на уровне спинного и среднего мозга. В этом периоде функции детрузора и сфинктера обычно хорошо сбалансированы.
По мере роста ребенка при формировании взрослой модели мочеиспускания (к 2, 5 – 3 годам) [1] имеют значение 3 фактора. Первый – увеличение емкости мочевого пузыря (в 6 раз) с урежением частоты мочеиспусканий; второй – приобретение контроля над сфинктером и другими уретальными механизмами, ответственными за начало и прекращение микции; третий – появление торможения мочеиспускательного рефлекса,что осуществляется ингибиторными кортикальными и субкортикальными центрами. До указанной вехи отличительной особенностью созревания акта мочеиспускания является повышение внутрипузырного давления в фазу накопления по сравнению с более старшими детьми. С 1,5-летнего возраста большинство детей приобретают способность чувствовать наполнение мочевого пузыря [2]. Кортикальный контроль над субкортикальными центрами устанавливается в возрастном периоде между 3 и 5 годами [3]. В связи с этим большинство случаев дисфункций мочеиспускания приходится на возраст 3 – 7 лет.
Рис. 1. Клинические симптомокомплексы нейрогенных дисфункций мочевого пузыря
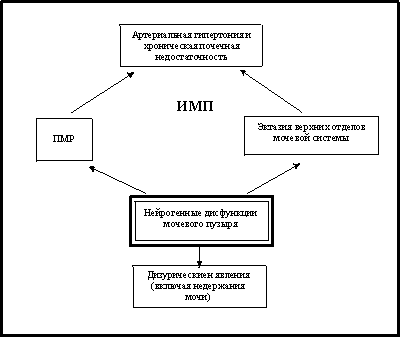
Наиболее частый вариант дисфункций мочевого пузыря – нестабильный мочевой пузырь – обусловлен сохранением незаторможенных сокращений детрузора вследствие замедленного созревания микционного (ингибиторного) центра в коре головного мозга или ретикулоспинальных путей. Возможной причиной указанного патологического типа мочеиспускания является перинатальная энцефалопатия, а также один из ее исходов – детский церебральный паралич, при котором гиперрефлексная детрузора может быть единственным проявлением.
Подчеркивается определенное неблагоприятное влияние эстрогенов на уродинамику верхних и нижних отделов мочевых путей. В частности, гиперрефлексия у девочек с нестабильным мочевым пузырем сопровождается нарастанием эстрогенной насыщенности, обусловливающей повышение чувствительности М-холинорецепторов к ацетилхолину [4]. Это объясняет преобладание детей женского пола в совокупной группе больных с расстройствами мочеиспускания функциональной природы.
В условиях недостаточно ингибированного автоматизма мочевого пузыря при отсутствии адекватной релаксации наружного сфинктера происходит повышение внутрипузырного давления. Подобная диссинергия возможна и в тех случаях, когда ребенок на фоне гипертонуса мочевого пузыря старается удержаться сухим волевыми усилиями. В сложившейся ситуации возникает вероятность развития несостоятельности замыкательного механизма уретеровезикального соустья, обеспечивающего в нормальных условиях антирефлюксную защиту [5]. Возникающий при этом пузырно-мочеточниковый рефлюкс (ПМР) представляет основную опасность нейрогенных дисфункций в отношении повреждения верхних отделов мочевого тракта.
Принимая во внимание большую вероятность обусловленности ПМР нейрогенными дисфункциями мочевого пузыря, все чаще приходят к мнению о консервативном ведении больных с рефлюксом на фоне применения антихолинергетиков и мероприятий, улучшающих уродинамику. Подобная тактика значительно повышает частоту разрешения ПМР у детей первых лет жизни и улучшает исходы антирефлюксных операций [5, 6]. S. Greenfield и J. Wan [7] предлагают усредненный срок наблюдения за ПМР – 4 – 5 лет (возраст становления взрослой модели мочеиспускания), после которого в случае его сохранения должно быть предпринято хирургическое вмешательство.
| · недержание мочи ночью и днем · хронические запоры и энкопроз · рецидивирующая ИМП · отсутствие анатомических аномалий верхних и нижних мочевых путей, а также неврологической патологии · особенности психического статуса: недостаток индивидуальности. Неблагоприятное психологическое окружение · снижение азотовыделительной функции почек с развитием хронической почечной недостаточности. Артериальная гипертензия · рентгенологические изменения: уретеровезикальная обструкция, ПМР, дилатация верхних отделов мочевой системы, рубцы в почках, вторично-сморщенная почка положительное влияние воспитания, суггестивной терапии и тренинга мочевого пузыря · безуспешность восстановительной хирургии |
Другое возможное тяжелое последствие в условиях высокого давления в мочевом пузыре – гидронефроз, развитие которого объясняют констрикцией пузырно-уретрального сегмента на фоне детрузорной гипертрофии [8].
Потеря функциональной целостности детрузора, шейки мочевого пузыря и наружного сфинктера является причиной возникновения дизурических расстройств (в частности, недержания мочи), тип и характер которых определяется доминантой активности указанных мышечных образований. Отягощают нейрогенные дисфункции мочевого пузыря инфекции мочевыводящих путей (ИМП) любой локализации. В то же время они могут инициировать некоторые варианты дисфункций мочеиспускания [9].
Таким образом, указанная патология может сопровождаться только расстройствами мочеиспускания, не вызывающими серьезных отклонений в здоровье ребенка и доставляющими лишь чувство дискомфорта. Однако потенциально возможны более тяжелые последствия (рис. 1).
Классификация
Нисколько не умаляя достоинств классификации нейрогенных дисфункций мочевого пузыря, представленной в великолепной монографии под редакцией М.Д. Джавад-Заде и В.М. Державина [10], необходимо отметить, что она базируется на сугубо функциональных характеристиках, оценка которых проводится с помощью специальных методов (хотя бы – цистометрии). Нет сомнений в необходимости использования тестов для исследования уродинамики у больных с нарушениями мочеиспускания в целом ряде случаев. Тем не менее в широкой клинической практике, включая нефрологические и урологические стационары, технологии по детализации функций мочевого пузыря обычно отсутствуют.
Кроме того, данная классификация не предполагает подразделение вариантов дисфункций мочеиспускания на угрожающие (в отношении повреждения вышележащих отделов мочевой системы) и значительно более легкие моносимптомные состояния только с дизурическими расстройствами. Выделение указанных вариантов по клиническому симптомокомплексу позволяет определять объем диагностических процедур.
Привлекательность классификации Y. Homsy [11] заключается в разделении дисфункций мочевого пузыря по тяжести, на основании вероятности вовлечения верхних отделов мочевой системы. Кроме того, учитывается функциональная целостность активности детрузора и наружного сфинктера. Подобный подход, по нашему мнению, наиболее близок практикующим педиатрам (табл. 1).
Рис. 2. Цистометрические показатели.
Первый +отмечает первый позыв на мочеиспусканье, второй +-императивный позыв
 |
а – здоровый ребенок (11 лет). Объем ретроградно введенной жидкости (V) и давление в мочевом пузыре (Р) укладываются в возрастные нормативы (V+ = 146 мл, V++ = 238 мл; Р+ = 8,2 см Н2О, Р++ = 12,7 см Н2О). Отсутствуют значительные перепады давления в мочевом пузыре при его наполнении, характеризующие степень адаптационных процессов (А+ = 88%, А++ = 79%); |
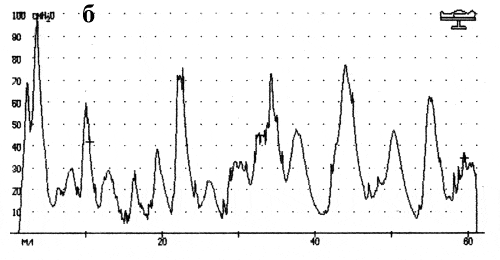 |
б – больной ребенок (5 лет) с гиперрефлекторным неадаптированным мочевым пузырем. Низкий объем наполнения при первом (V+ = 7 мл) и императивном (V++ = 65 мл) позывах. Повышенное давление в мочевом пузыре (Р+ = 36,5 см Н2О, Р++ = 29,1 см Н2О). Значительные колебания внутрипузырного давления в фазе накопления (А+ = –17%, А++ = 23%). |
Клиника
Синдром дневного частого мочеиспускания (СДЧМ). Впервые описан S. Kоff и M. Byard в 1988 г. [12]. Клинические проявления заключаются во внезапном появлении частых позывов на мочеиспускание (через 15 – 20 мин). Микция при этом безболезненная, и уродинамическое обследование не выявляет значительных отклонений. Указанный симптомокомплекс может сохраняться от 2 дней до нескольких месяцев и обычно ликвидируется спонтанно, в то же время, уступая антихолинергетикам.
Стрессовое недержание. Редкий вариант дисфункций мочеиспускания, проявляющийся у девочек пубертатного возраста при напряжении в момент выполнения гимнастических упражнений. Обычно упускаемые порции мочи очень небольшие. Профилактика этой легкой дисфункции сводится к опорожнению мочевого пузыря перед физической нагрузкой.
Недержание мочи при смехе. Распространено среди девочек предпубертатного и пубертатного возраста и иногда сопровождается полным опорожнением мочевого пузыря. При исследовании уродинамики в редких случаях обнаруживают неингибированные сокращения мочевого пузыря (гиперрефлекторный мочевой пузырь). Это самоликвидирующееся состояние может уступать антихолинергетикам или симпатомиметикам.
Ночной энурез. Моносимптомное состояние, в 3 раза чаще встречающееся у мальчиков и связанное, по-видимому, с нарушением процессов созревания кортикальных механизмов, обеспечивающих произвольный контроль за рефлексом мочеиспускания. Первичный энурез (в случае отсутствия периода удерживания мочи в ночное время) чаще обусловлен перинатальной энцефалопатией. Патология может носить вторичный характер после эмоционального стресса, на фоне болевого синдрома, переутомления, интоксикации при тяжелых соматических и инфекционных заболеваниях.
Инструментальное обследование лишь в редких случаях выявляет гиперрефлексию мочевого пузыря, особенно в ночное время. Однако эпизоды энуреза не совпадают с цистометрическими показателями. Ночной энурез редко сопровождается ПМР, частота которого значительно нарастает в случае сочетания ночного и дневного недержания мочи.
До начала проведения терапии необходимо исключить ряд патологических состояний, способных протекать с энурезом (табл. 2).
В настоящее время для лечения энуреза начали использовать десмопрессии (дезамино-Д-аргинин вазопрессии – ДДАВП) ввиду установленной связи указанного состояния с замедлением становления нормального циркадного уровня секреции антидиуретического гормона (АДГ). Заместительная терапия этим препаратом снижает частоту случаев энуреза у детей с дефицитом АДГ. Однако необходимо подчеркнуть, что ДДАВП не излечивает от энуреза, и часто его эффект не превышает продолжительности терапии. Кроме того, еще не оценены отдаленные результаты такого лечения. Комплексная терапия ночного энуреза, представленная далее в статье, дает положительные результаты в 60 – 80% случаев.
Синдром ленивого мочевого пузыря. Чаще встречается у девочек и характеризуется редкими мочеиспусканиями через 8 – 12 ч, которые могут перемежаться недержанием мочи. При этом нередко отмечаются запоры, а длительная задержка мочи в мочевом пузыре приводит к развитию инфекции нижних отделов мочевой системы. Мочеиспускание у данной категории детей требует дополнительных усилий со стороны мышц передней брюшной стенки, но даже при этих условиях оно нередко носит прерывистый характер и не сопровождается полным опорожнением мочевого пузыря.
Этиологически редкие мочеиспускания могут иметь поведенческий характер, или лежащий в их основе явный дефицит детрузорной активности (гипорефлексия). Признаков инфравезикальной обструкции не отмечают. Особенностью лечения является обеспечение частого мочеиспускания (через 2 ч), а для полной эвакуации мочи – двойное мочеиспускание. В случае больших количеств остаточной мочи рекомендуются периодические катетеризации. В редких случаях указанная дисфункция сочетается с эктазией верхних отделов мочевой системы.
Нестабильный (гиперрефлекторный) мочевой пузырь. Наиболее частая из дисфункций мочеиспускания патология, которая обусловлена нарушениями уродинамики. Она связана с замедлением исчезновения незаторможенных сокращений мочевого пузыря. Автоматическому режиму работы, изгоняющему мочу из мочевого пузыря, могут препятствовать сокращения наружного сфинктера, произвольный контроль над которым устанавливается в раннем детстве. В частности, подобная ситуация возникает, когда ребенок хочет остаться сухим и удержаться от мочеиспускания. Это отдаленно напоминает расстройства уродинамики при клапанах задней уретры.
Таблица 6. Терапевтические мероприятия при нейрогенных дисфункциях мочевого пузыря
| Вид нейрогенной дисфункции |
Мочеиспускания по графику |
Периодические катеризации* |
Витаминотерапия |
Антихолинергетики |
Психотропные и седатативные средства |
Антибактериальная профилактика*** |
Физиотерапия*** |
Другие методы |
| СДЧМ |
– |
– |
– |
+** |
– |
– |
– |
– |
| Недержание мочи при смехе |
– |
– |
– |
+** |
– |
– |
– |
– |
| Ночной энурез |
– |
– |
+ |
+ |
+ |
– |
+ |
Десмопрессин** |
| Синдром ленивого мочевого пузыря |
+ |
+ |
+ |
– |
– |
– |
+ |
М-холиномиметики (ацеклидин) Слабительные |
| Нестабильный (гиперрефлекторный) мочевой пузырь |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
Биологическая обратная связь |
| Синдром Хинмана |
+ |
+ |
– |
+ |
+ |
+ |
+ |
Биологическая обратная связь Слабительные Психотерапия |
| Синдром Очоа |
+ |
+ |
? |
+ |
? |
+ |
? |
? |
| *При большом количестве остаточной мочи и/или обострении ИМП на фоне ПМР. **Альтернативные показания. ***При ИМП для профилактики рецидивов. ****Расшифровка в тексте. ? нет данных об эффективности. |
||||||||
Таким образом, нестабильный мочевой пузырь создает условия для повышения внутрипузырного давления, которое, в свою очередь, может обусловить возникновение одно- или двухстороннего ПМР (у 30 – 50% больных), нередко с развитием рефлюкс-нефропатии. У этой категории детей обычно отсутствует недержание мочи, нередко имеет место обструкция уретеровезикального сегмента, приводящая к расширению мочеточника и лоханки [8]. Указанные варианты нестабильного мочевого пузыря, протекающие с выраженной детрузорной гиперконтрактильностью, наблюдаются у детей различных возрастных групп, включая первые месяцы жизни. Эта группа больных часто не уступает лечению антихолинергетиками.
У 60 – 70% детей активность детрузора преобладает над резистентностью наружного сфинктера, и указанная дисфункция манифестирует частыми императивными и/или болезненными позывами, непроизвольным мочеиспусканием, ночным энурезом. Независимо от вариантов гиперрефлексии часто встречается рецидивирующая ИМП. В большинстве случаев антихолинергетики, принудительные мочеиспускания, периодические катетеризации вызывают разрешение ПМР или способствуют снижению его тяжести [5, 6, 13].
Синдром Хинмана. Данный симптомокомплекс впервые описан F. Hinman и F. Bauman в 1973 г. [14] и является самым тяжелым вариантом детрузорно-сфинктерной диссинергии. Клиническая картина представлена в табл. 3.
Эта достаточно редкая патология уникальна в отношении развития необратимых изменений почек на фоне функциональных нарушений акта мочеиспускания, когда отсутствуют механические признаки обструкции, являющиеся основными причинами нефросклероза в детской практике. В данном случае возникающая обструкция обусловлена недостаточным расслаблением наружного сфинктера при попытке мочеиспускания, что при исследовании уродинамики подтверждается снижением скорости потока мочи, нарастанием времени опорожнения, повышенным либо уменьшенным внутрипузырным давлением, наличием резидуальной мочи, а также большого мочевого пузыря с утолщенными стенками [15].
Предполагается участие психологического компонента в развитии указанной дисфункции, принимая во внимание особенности психического статуса и неблагоприятный семейный анамнез (алкоголизм, психические травмы, недостаток воспитания и др.) у данной категории больных. Психотерапия детей и в семьях нередко позволяют улучшить уродинамику [15].
D. Varlam и J. Dippell [15], наблюдая 9 девочек с синдромом Хинмана в течение 5 лет, у 8 из них установили высокие уровни креатинина с развитием терминальной почечной недостаточности в 1 случае. У 5 детей отмечалась артериальная гипертензия (включая гипертонический криз).
Показано 2-этапное ведение подобной категории больных. Первый (симптоматический) – направлен главным образом на нормализацию уродинамики и включает периодические катетеризации мочевого пузыря, частые мочеиспускания с применением метода биологической обратной связи, антихолинергетики, слабительные средства, антимикробную профилактику ИМП, а также отведение мочи из лоханки при гидронефрозе. Р. Гонзалез и А. Микаэль [9] для расслабления сфинктера рекомендуют применение диазепама (седуксена). Второй этап (этиологический) заключается в проведении суггестивной терапии и воспитательных мероприятий (гигиенические навыки).
Синдром Очоа (урофациальный синдром). Описан в Колумбии, и частота его в других странах еще не известна. Синоним данной патологии – урофациальный синдром, обусловлен инверсией выражения лица при смехе, создающей впечатление крика или плача. Существует гипотеза, которая объясняет взаимосвязь выражения лица и расстройств функции мочевого пузыря. Она заключается в предположении о близости центров мочеиспускания и лицевого нерва в стволе головного мозга, и нарушения в этой области могут затрагивать некоторые органные функции.
Данный симптомокомплекс имеет много общих особенностей с синдромом Хинмана. Возраст больных – от 3 мес до 16 лет. Предполагается аутосомно-рецессивный тип передачи [16]. Клиническая картина характеризуется дневным и/или ночным энурезом, хроническими запорами, рецидивирующей ИМП, высокой частотой ПМР и уретерогидронефроза (вследствие функциональной уретеровезикальной обструкции) [17]. Синдром Очоа представляет угрозу развития гипертензии и хронической почечной недостаточности. Цистометрические исследования устанавливают незаторможенные сокращения мочевого пузыря и большое количество остаточной мочи. Лечебная тактика урофациального синдрома сходна с синдромом Хинмана.
Диагностика
Объем диагностических процедур включает проведение обязательных мероприятий, которыми можно ограничиться при наличии легких нарушений мочеиспускания, а также специальных методов по показаниям (табл. 4). Комплекс последних позволяет исключить прогностически неблагоприятные последствия нейрогенного мочевого пузыря (ПМР, эктазию верхних отделов мочевой системы, артериальную гипертонию, снижение парциальных функций почек), а также первичные заболевания, которые могут сопровождаться расстройствами мочеиспускания (эктопированное устье мочеточника, инфравезикальная обструкция).
Таким образом, нередко возникает ситуация, требующая комплексного обследования ребенка с включением инструментальных методов (в том числе используемых обычно в урологической практике). Имеется в виду прежде всего оценка функции уродинамики нижних мочевых путей на основе проведения урофлуометрии, цистометрии, профилометрии и электромиографии. Это можно осуществить с помощью прибора "Рельеф" (Россия), собственный опыт использования которого на базе Детской городской больницы Святого Владимира начат с 1994 г. Данное устройство позволяет оценить не только функциональные варианты дисфункций [10], но и исключить механические препятствия в уретре.
На основании исследования уродинамики была предложена классификация нейрогенных дисфункций мочевого пузыря (табл. 5) [10], варианты которых представлены в убывающей по частоте последовательности. Понятие гиперрефлексии имеет в виду повышенную возбудимость спинальной дуги мочеиспускания.
Адаптированность мочевого пузыря является его свойством сохранять уровень давления на минимально возможном при поступлении единицы объема жидкости. Напротив, неадаптированный (незаторможенный) мочевой пузырь характеризуется неадекватным повышением давления, нарушающим зависимость между ним и объемом. Нарушения уродинамики, проявляющиеся в положении сидя или стоя, относятся к постуральным. На рис. 2 приведены результаты оценки уродинамики в режиме цистометрии у здорового ребенка (а) и при самой частой дисфункции – гиперрефлекторном неадаптированном мочевом пузыре (б).
Лечение
Лечение нейрогенных дисфункций мочевого пузыря нередко является сложной задачей, требует комплексной терапии и предполагает дифференцированную тактику (табл. 6).
Общие мероприятия. Рекомендуется охранительный режим с устранением психотравмирующих ситуаций, дополнительным сном (1 – 2 ч), отказом от бурных игр перед сном, вызывающих ночной энурез, прогулками на свежем воздухе. При наличии резидуального фона клиническое наблюдение проводится совместно с невропатологом.
Уростаз в мочевом пузыре требует проведения периодических катетеризаций, а также мочеиспусканий по расписанному графику (в случае гипорефлекторного мочевого пузыря с двойным или тройным его опорожнением).
Витаминотерапия. Витамины группы В (В1,В2, В6), РР, А и Е в возрастных дозировках комплексно с возможным парентаральным введением.
Антихолинергетики. Избирательно при гиперрефлексии (один из препаратов):
беллатаминал – по 1/2 – 1 таблетке 2 раза в день;
оксибутинин – у детей старше 5 лет по 1 таблетке (5 мг) 2 раза в день (3 раза с последней дозой на ночь при ночном энурезе);
мелипрамин – по 0,02 – 0,05 г 1 раз на ночь или по 0,01 – 0,025 г в 16 и 20 ч. Лечебной дозы достигают постепенно, начиная с 0,01 г. Помимо антихолинергического действия обладает миотропной спазмолитической и антидепрессантной активностью;
атропин – по 0,05 – 0,5 мг 1 или 2 раза в день. Для прогностической оценки эффективности указанных средств используют атропиновую пробу, положительные результаты которой (улучшение показателей уродинамики через 30 – 40 мин после подкожного введения атропина) являются показанием к назначению антихолинергетиков.
Средства, нормализующие обменные процессы в ЦНС
Аминокислоты:
глутаминовая кислота – по 0,25 – 1 г 2 раза в день;
глицин – 0,05 – 0,1 г 3 раза в день;
Ноотропы:
пирацетам – до 5 лет – по 0,2 г 3 раза в день, старше 5 лет – по 0,4 г 3 раза в день или 20% раствор по 8 мл 2 раза в день;
пикамилон – по 0,01 – 0,025 г 2 раза в день;
пантогам – по 0,25 – 0,5 г 3 раза в день.
Продолжительность курсов витаминотерапии, антихолинергетиков, аминокислот, ноотропов составляет 1 – 1,5 мес с последующим 1 – 2-кратным повторением с интервалом 4 – 6 нед. Для исключения большого объема одновременно принимаемых внутрь лекарственных средств показано их последовательное назначение.
Седативные препараты
Преимущество отдают препаратам растительного происхождения (валериана, пустырник), которые даются перемежающими курсами по 2 нед на протяжении 2 мес.
диазепам – по 0,0025 – 0,005 г 2 раза в день рекомендуется назначать при синдроме Хинмана, принимая во внимание миорелаксирующее действие;
либракс – по 1/2 – 1 драже 2 раза в день (в том числе при ночном энурезе, когда 2-я доза дается перед сном). Спектр действия препарата включает также антихолинергический эффект.
Антибактериальная профилактика ИМП
При обострении ИМП любой локализации назначают этиотропную терапию, эффективность которой повышается по мере нормализации уродинамики. Метод антибактериальной профилактики ИМП в периоде ремиссии обосновывается отчетливой зависимостью нефросклеротических процессов от частоты обострений, особенно при наличии ПМР [18]. Кроме того, персистирующая инфекция в нижнем отделе мочевой системы способна поддерживать дисфункции мочевого пузыря.
Номенклатура профилактических средств включает уросептики в малых дозах: фурагин (или другие нитрофураны) – 1 мг/кг, ко-тримоксазол – 12 мг/кг, невиграмон – 15 мг/кг. Их дают однократно на ночь длительными многомесячными курсами.
Нами показана эффективность противорецидивного назначения иммунокорригирующих препаратов: левамизола (1 мг/кг) 1 раз в неделю, а при интеркуррентных заболеваниях 3-дневным циклом с последующим приемом 1 раз в неделю в течение 1 – 2 мес; тактивина (2 мкг/кг) 3-дневным циклом с последующими 3 инъекциями с интервалом 1 – 2 дня при сопутствующих заболеваниях; нуклеината натрия (0,05 – 0,1 г 3 раза в день) курсами по 1 – 2 мес [19].
Другие мероприятия. Некоторые особенности ведения детей в зависимости от вида дисфункции мочеис




